编译:高杰
你有没有发现?
同样类型的伤口,
长在脸上和长在身上,
愈合结局完全不一样——
脸上的伤口愈合快、疤痕浅,
几乎不影响外观;
而身体其他部位的伤口,
却常常留下难以消退的瘢痕。
这背后究竟隐藏着什么
生物学奥秘?
斯坦福大学研究团队通过严谨的小鼠创伤模型实验,首次系统揭示了不同部位伤口愈合差异背后的细胞与分子机制,相关成果在《细胞》上发表。
研究团队在小鼠面部、头皮、腹部和背部皮肤均制造了切除性伤口,术后组织学评估显示:面部伤口愈合后瘢痕最轻,真皮结构更接近正常皮肤;而背部伤口愈合后瘢痕最重,纤维化程度最为显著。这一发现与临床观察高度一致——人体面部伤口确实比其他部位更容易实现“无痕”愈合。

伤口愈合的核心执行者是成纤维细胞,它负责合成胶原、重塑组织,也直接决定瘢痕轻重。为了探究不同部位差异的根源,研究人员对伤口愈合不同阶段的组织进行了单细胞RNA测序。结果显示,面部成纤维细胞与其他部位的成纤维细胞在基因表达上存在显著差异。
面部成纤维细胞,在胚胎阶段来源于颅神经嵴细胞;而头皮、腹部、背部的成纤维细胞,均来自不同类型的中胚层。
进一步基因分析显示,面部成纤维细胞中,Robo2基因及其下游靶基因Eid1的表达水平显著更高。为验证这一结论,团队开展了细胞移植实验:将面部成纤维细胞移植到背部伤口,瘢痕宽度明显减小、胶原沉积减少,纤维化程度显著改善。反之,若敲除面部成纤维细胞中的Robo2或Eid1,其低瘢痕特性便会完全消失。
这一结果直接证实:发育起源决定了成纤维细胞的固有纤维化能力,而Robo2与Eid1是维持面部低瘢痕表型的关键基因。
那么,Robo2和Eid1究竟如何发挥“抗瘢痕”作用?研究揭示了一条清晰的信号通路:ROBO2-EID1-EP300。
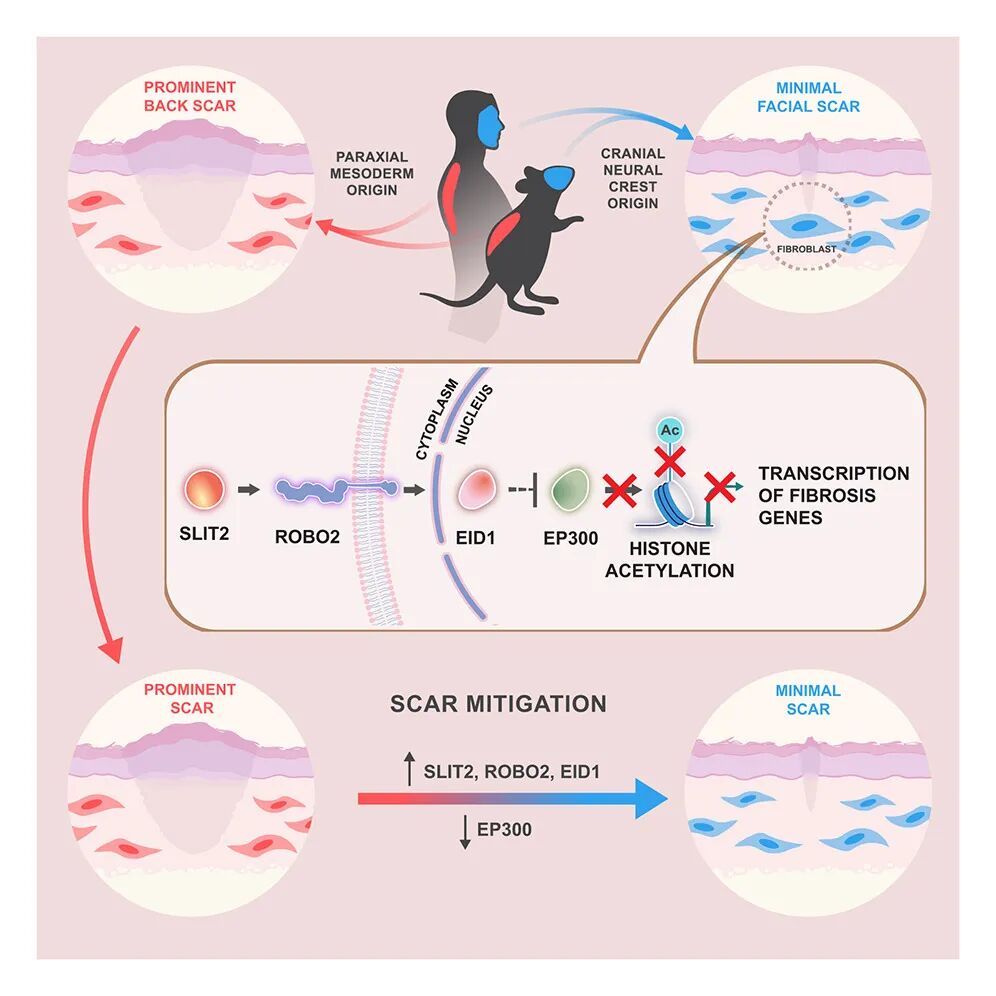
Eid1编码的EID1蛋白能够抑制组蛋白乙酰转移酶EP300的活性。EP300是调控基因转录的关键表观遗传修饰酶,其活性降低会导致染色质处于更加沉默的状态,尤其是Col1a1、Col3a1、Fn1等促纤维化、促胶原沉积的基因表达被显著削弱,最终实现低瘢痕、轻纤维化的愈合模式。
这一机制的发现具有直接的临床转化价值。研究团队尝试通过两种策略模拟EID1的活性:一是使用小分子药物抑制EP300,二是通过转基因手段在成纤维细胞中特异性敲除EP300。
结果显示,这两种方法均能使背部伤口呈现出类似面部的愈合特征——瘢痕减少、纤维化程度降低。分子层面,细胞外基质基因区域的H3K27乙酰化水平也明显下降。
这意味着,即便细胞发育起源无法改变,依然可以通过靶向调控EP300,让易留疤部位实现面部级“无痕”愈合。

这项研究不止解释了一个生活常识,它首次证明,成纤维细胞的胚胎发育起源赋予其内在的纤维化潜能,而这种潜能可以通过干预特定的表观遗传通路进行调控。
正如斯坦福大学医学院Michael T. Longaker教授所言:“瘢痕形成并非无规律可循,这项研究以及实验室此前的发现表明,无论组织类型如何,都存在共同的调控机制和关键分子。”这意味着,针对EP300等靶点的治疗策略,可能不仅适用于皮肤瘢痕,还有望拓展至内脏纤维化等更多疾病领域。
目前,该研究主要基于小鼠模型,EP300抑制剂的临床应用仍需经过严格的安全性评估。但毫无疑问,ROBO2-EID1-EP300信号轴为抗瘢痕药物研发提供了一个全新且极具前景的靶点。未来,或许只需在伤口局部应用能够模拟EID1功能或抑制EP300的小分子药物,就能让瘢痕易发部位获得类似面部的再生愈合能力。
数据图及参考来源:
https://www.cell.com/cell/abstract/S0092-8674(25)01427-8
除已标注来源外,本文封面图及文内图片均来自包图网(获授权使用),转载可能引起版权纠纷。