2024年5月3日,复旦大学附属中山医院樊嘉院士和高强教授、中国科学院上海免疫与感染研究所张晓明研究员、浙江大学基础医学院郭国骥教授合作在Science上发表了题为A blueprint for tumor-infiltrating B cells across human cancers的研究论文,结合单细胞转录组、 B细胞受体免疫组库和表观基因组的多组学数据,系统性地刻画了肿瘤浸润性B细胞的异质性、动态分化和表观调控机制。创新地揭示了肿瘤微环境中广泛存在的EF应答的癌种偏好性、空间定位特征、临床意义及潜在的诱导调控机制。

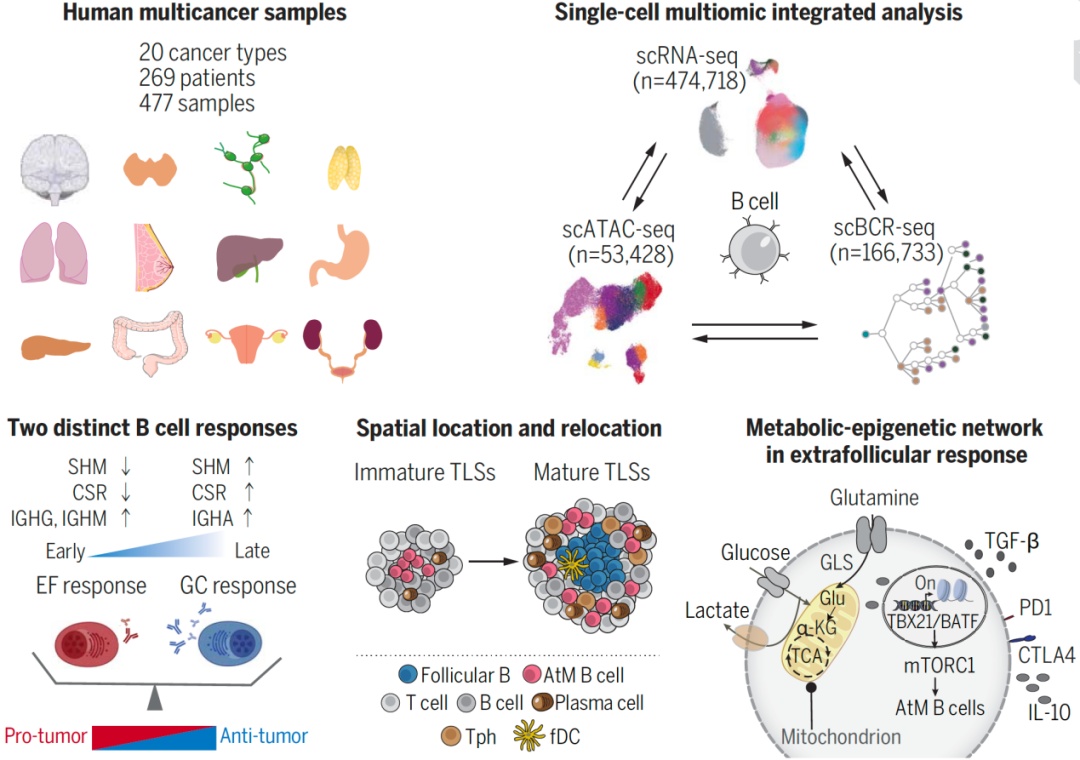
在这项研究中,研究者通过整合自测数据(69.24%)和公共数据共20个癌种的269例患者共计477例样本的B细胞单细胞转录组,利用聚类分析发现B细胞可分为15大群,其中四个新的亚群为首次报道,包括IFIT3+炎症B细胞、HSPA1A+应激B细胞、DUSP4+非典型记忆B细胞和pre_GCB细胞。同时还发现,肿瘤浸润的浆细胞在多个层面的存在异质性,可分为10个不同的亚群。重要的是,浆细胞的分化主要来源于GC和EF应答两种不同途径,并且具有明显的癌种偏好性。例如,肝癌主要由EF应答驱动,而结直肠癌则主要由GC应答驱动。研究者还深入比较了这两种来源的浆细胞在转录组、BCR免疫组库和表观遗传调控等方面的差异。通过单细胞轨迹算法、流式细胞和多重免疫荧光标记等技术,阐明了EF来源浆细胞的早期应答特征,而GC来源的浆细胞则呈现出晚期应答特征。
研究者进一步聚焦EF来源浆细胞的前体细胞——DUSP4+非典型记忆(AtM)B细胞,细致的描绘了其在肿瘤中的表型、功能、空间定位和调控机制。研究发现,AtM B细胞表现为耗竭和旁观的表型,分泌识别自身抗原的抗体,并且其分化途径独立于GC。研究还揭示了AtM B细胞与早期不成熟的TLSs相关,定位于不成熟TLSs的中心,在成熟TLSs中迁移到外周(滤泡外)。进一步发现,PD1HiCD4+Tph细胞(外周辅助T细胞)与AtM B细胞在空间上共定位,并通过IL21-IL21R轴诱导AtM B细胞分化。
最后,研究者通过单细胞代谢通路分析、非靶向质谱和体外诱导等技术,发现谷氨酰胺衍生的代谢物α-酮戊二酸会增加B细胞的H3K27三甲基化,激活哺乳动物雷帕霉素靶复合物1(mTORC1)信号通路,促进AtM B细胞相关转录因子Tbet和BATF的表达,促进AtM B细胞分化。功能研究发现,AtM B 细胞获得了抑制T细胞的免疫调节功能,最终导致免疫抑制的肿瘤微环境形成,在多个癌种的临床队列中,AtM B 细胞与较差的临床预后和免疫治疗抵抗显著相关。
针对这项研究,Science同期发表了澳大利亚墨尔本大学和WEHI研究所Stephen L. Nutt教授(澳大利亚科学院院士)的评述:“本研究无偏移的解码了B细胞在肿瘤微环境中存在两种不同的成熟分化轨迹,并证明了这种分化具有癌种特异性和代谢表观调控机制。这一发现揭示了体液免疫在肿瘤免疫中的复杂作用,阐明了B细胞的分化轨迹及其所在肿瘤微环境的综合特征,共同决定了肿瘤的临床预后和疗效。该研究提示了激发肿瘤特异性B细胞反应的治疗价值,并为开发新型免疫疗法提供了坚实的理论支持。”

复旦大学附属中山医院樊嘉院士和高强教授、中国科学院上海免疫与感染研究所张晓明研究员、浙江大学基础医学院郭国骥教授为本文通讯作者。复旦大学博士生马家强、吴英成、杨旭鹏、硕士生张天成和浙江大学博士生马立枫为共同第一作者。本研究得到中国科学院分子细胞科学卓越创新中心李党生研究员、复旦大学施思教授和王玉龙教授、上海交通大学黄陈教授、苏州血液中心汤龙海教授和王明元教授的支持。
本项目得到国家自然科学基金委、中国科学院和上海市科委相关计划资助。
原文链接:
https://doi.org/10.1126/science.adj4857
来源:BioArt
编辑:zy
↓分享
↓点赞
↓在看